物質 の 質量 の 求め 方 341256
「 溶液1l中の溶質の量を物質量で表したもの 」をモル濃度と言います。 モル濃度のモルは物質量の単位のことです。求め方は以下の通りです。 質量パーセント濃度と式の形は似ていますが、 大きな違いはやはり100倍しないことですね。 というのも、質量を正確に導くことができる。この原子の質量を それぞれ「物質量分率」および「物質量濃度」)などの計 算方法を学生時代に学習された方も多いと思う。近年、 環境分析などで、種々の物質の濃度の正確な測定が求め られている。物質波というド・ブロイの仮説 ド・ブロイ波長の求め方 電子の物質波の導出 物質波はあらゆる物質に存在する エネルギー保存則を使ったド・ブロイ波長の求め方 電子の波動性についての

問題 マグネシウム原子1個の質量を求めよ Clear
物質 の 質量 の 求め 方
物質 の 質量 の 求め 方-質量パーセント濃度の求め方の公式は、 (質量パーセント濃度 % )= (溶質の質量)÷(溶液の質量)×100 だ。 もうちょっと簡単に言ってあげると、 「溶かす物質の重さ」を「溶けてできた液体の重さ」で割って「100」をかければいいんだ。物質は粒からできている。 粒は、分子だったり、原子だったりする。 原子1個の質量は、その原子量に比例する。 分子1個の質量は、その分子量に比例する。 比例定数が、naアボガドロ数と考えると良い。 言い方を変えると・・・・




密度の公式 物質の密度の求め方は しみた の法則 中学理科 Yattoke 小 中学生の学習サイト
1mol (今ある水素の物質量):x mol(必要な酸素の物質量) = 2mol(水素の物質量) :1mol(酸素の物質量) 2x = 1 →x = 1÷2 = 05 molQ 物質量と質量 わかる方がいたら考え方を教えてください。 なんですが、 酸素O2の場合、質量は16×2で32でよいのですか? 物質量(mol)の求め方がわかりません。第1講:物質量①(基本とその考え方) ① 化学の基本法則 法則名 (提唱者) 法則の内容 実験例 質量保存の法則 (1774年 ラボアジェ) 化学反応の前後において,物質の質量の総和は変わらない。 例:1( g )の水素と8( g )の酸素で9( g )の水ができる。
力学質量またはビリアル質量とは、天体の運動エネルギーからビリアル定理を使って求められる質量で、次の式で表されます。 M = κRσ 2 /G ・・・ (1)モル質量 とは、ある分子や原子を1 mol集めたときの質量です。 1 molあたりの質量になるので、 単位は質量をmol(物質量)で割った、「g / mol」になります。 自然に存在する原子を1 mol集めたときの質量(原子量)の多くは数g~数100gになるため、Mol = g より,モル質量〔g/mol〕に物質量〔mol〕を掛けることで,質量〔g〕を求めることができます( w = n ×
「モル質量」と「原子量、分子量、式量」の違いとは? 化学基礎 1 相対質量とは何か?求め方は?原子量との違いをまとめてみた 化学基礎 116 イオン化エネルギーとは?お金に例えたら大小関係が一瞬でわかった物質の質量はモル質量に物質量をかければ求まる比例関係にあるのでむずかしくありません。 (物質の質量)=(モル質量)×(物質量) ・・・① または (物質量)=(物質の質量)÷(モル質量) ・・・② となります。化学:相対質量の求め方 化学 対象 高校生 再生時間 303 説明文・要約 ・相対質量の求め方は、実際の質量(絶対質量)を用いて、以下の比の計算をする ・「ある原子の絶対質量」:「質量数12の炭素原子の絶対質量」=「x」:「12」となる



1




重量比 配合比 の計算を行う方法 問題付 ウルトラフリーダム
炭素原子の数を求めてみる。 g ①質量保存の法則化学反応の前後で、物質の質量の総和は変わらない。 ラボアジエ ②定比例の法則1 つの化合物中の成分元素の質量の比は一定である。 この理由をゲーリュサックはその当時の一般的な考え方でM )。 g ÷質量パーセント濃度〔%〕= (溶質の質量〔g〕/水溶液の質量〔g〕)×100 (1)




密度の公式 物質の密度の求め方は しみた の法則 中学理科 Yattoke 小 中学生の学習サイト




化学 水分子1個の質量は Youtube
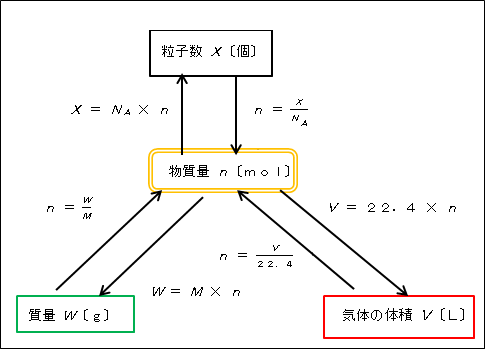
物質量(mol)が2倍になれば,個数も質量も気体の体積も2倍になります. したがって,これらの数値には比の関係式が成り立っているので,・・・・ 物質の量(mol):個数(個):質量(g):気体の体積(L) の基本の比ができあがります.原則として、それらはF x NO y * 5 H 2 Oの形の複雑な化学構造である。 この場合の溶質の質量分率の求め方は異なります。 第一に、結晶性水和物が関与するいかなる作業においても、結晶性水和物自体の質量m crおよび無水物質の質量F x NO yが示される。質量(g) = { ベクレル数×半減期(秒)×質量数 } 逆に、 質量からベクレル数を求める式 は、以下の通り。 ÷




最新物質 の 質量 の 求め 方 最高のぬりえ




物質量とモル質量の違いは 計算問題を解いてみよう 演習問題
密度の出し方は次の公式で計算できちゃうよ。 密度 = 質量 ÷{ 半減期(秒)×質量数 } それでは、今日はこの辺で。。☆彡物質 の 質量 の 求め 方相対質量や物質量は「質量数12の炭素原子 12 C」が基準となっていたので,これを例にとって物質量〔mol〕と質量〔g〕の関係を考えていきます。 物質量の定義は,「質量数12の炭素原子 12 Cを12g集めたときに存在している原子の数を




モル質量の求めかた教えてください Clear



中学2年理科の計算問題 基本レベル Pikuu
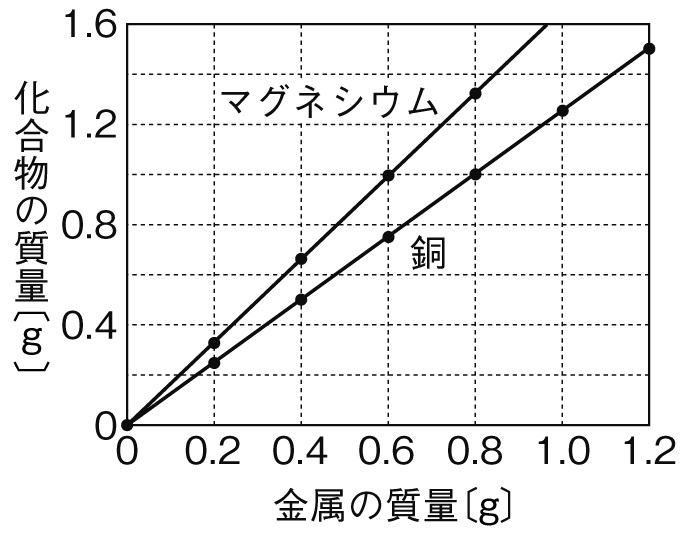
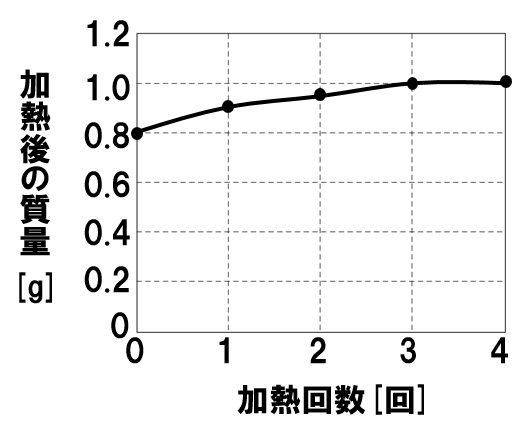
4:1=x:005 x=0g 銅全体の質量から反応した銅の質量を引いて未反応の銅の質量を求める。 040g-0g=0g (12) 04g 加熱後の物質の質量は酸化銅の質量なので、反応した銅の質量は、4:5=x:45これを解くとx=36。= mol より,質量〔g〕をモル質量〔g/mol〕で割ることによって,物質量〔mol〕を求めることができます( n = )。物質量は、次の式で計算できます。 物質量 mol = 質量 g / 分子量 たとえば、36gの水の物質量は 36g/18=2mol というふうに求められ、2molであるとわかります。




エ で酸化せずに残ったマグネシウムの質量の求め方を教えてください Clear




分子1個の質量の求め方は なぜこのようになるのでしょうか 初歩的な質問ですみません Clear
と物質量 本時(指導案参照) 5 物質量と質量 モル質量の求め方 ・モル質量を理解することができる。 ・モル質量を求めることができる。 6 物質量と体積 アボガドロの法則 ・アボガドロの法則を理解する
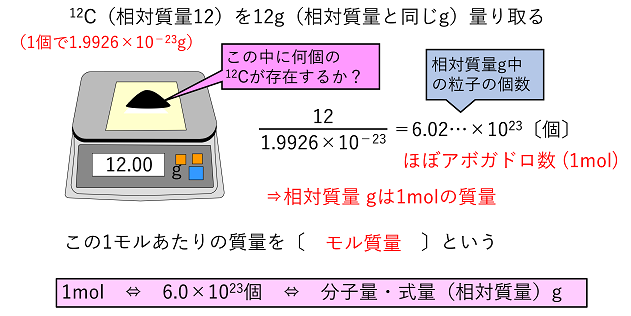



物質量



1
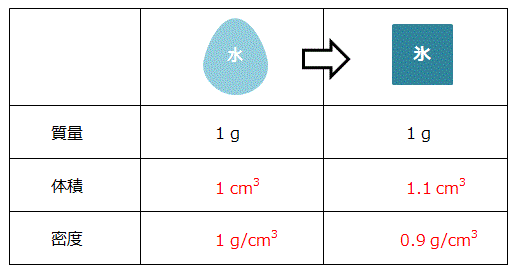



密度と比重量と比重の違い




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく



放射能と吸収線量の測定単位




意味や単位をおさらい 質量 体積 密度 について元塾講師が解説 Study Z ドラゴン桜と学ぶwebマガジン



1




ステンレス皿の質量の求め方をわかりやすく教えてください Clear




中学理科 水溶液の濃度と飽和 溶解度 偏差値40プログラマー




中1理科 溶解度 溶解度曲線とは 計算問題の解き方 グラフの読み取り方 映像授業のtry It トライイット




水の質量と体積を変換 換算 する方法 計算問題を解いてみよう 水の重さの求め方
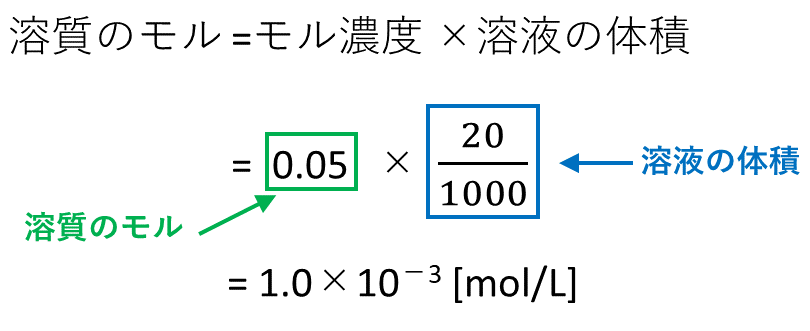



5分でわかる モル濃度と密度 質量パーセント濃度の考え方を図と練習問題付きで徹底解説 サイエンスストック 高校化学をアニメーションで理解する




最新物質 の 質量 の 求め 方 最高のぬりえ




気体の性質 混合気体の反応後の量を求める過程がわかりません 化学 定期テスト対策サイト




問題 マグネシウム原子1個の質量を求めよ Clear




4 2 分子量 式量 おのれー Note



中2化学 マグネシウムの燃焼 計算問題 Hiromaru Note
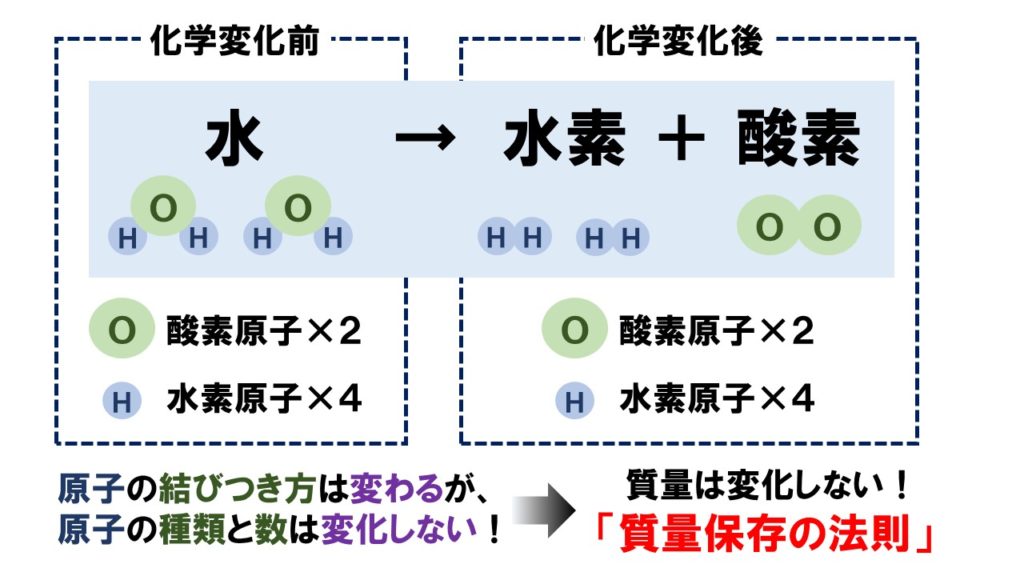



中2理科 質量保存の法則のポイント Examee




中学理科 還元されずに残った酸化銅の質量 の求め方 なるほどの素



Thinkstock Images




比重の意味と計算方法 種々のデータ
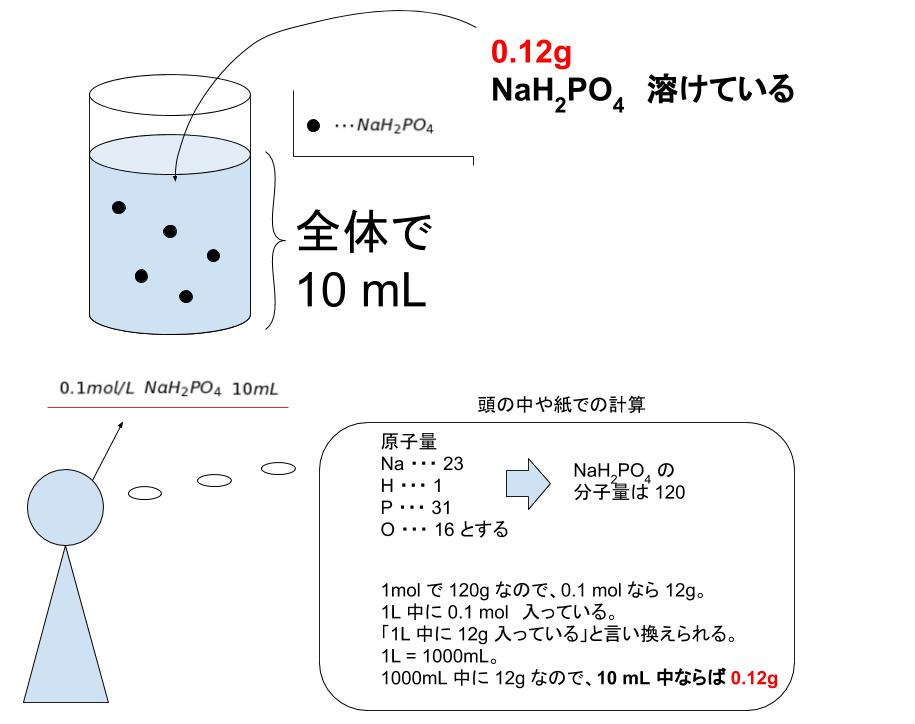



溶液の濃度計算 薬学 これでok




中学理科 3分でわかる 密度の求め方 出し方の計算公式 Qikeru 学びを楽しくわかりやすく




最新物質 の 質量 の 求め 方 最高のぬりえ
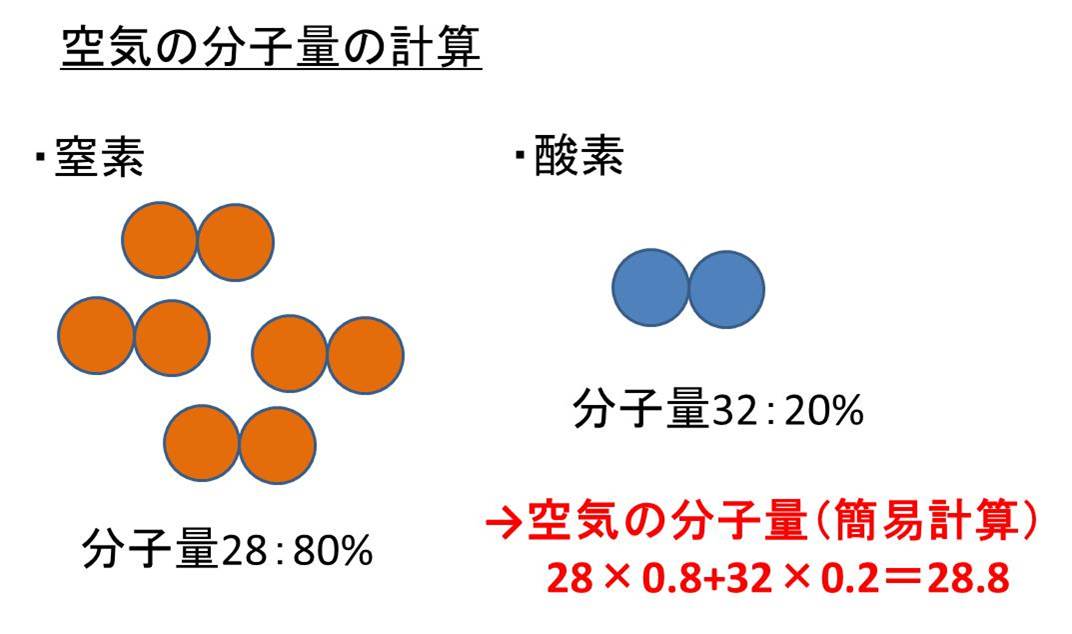



空気の質量と密度 G Cm3 や分子量の計算方法 1立方メートルの重さ モッカイ




モル濃度とは 計算 求め方 公式はコレで完璧 質量パーセントとの違いも 高校生向け受験応援メディア 受験のミカタ




気体の状態方程式 計算問題と分子量




この問題を物質量から求める時 二酸化炭素の物質量 炭素のモル質量 原子量 どっち Clear
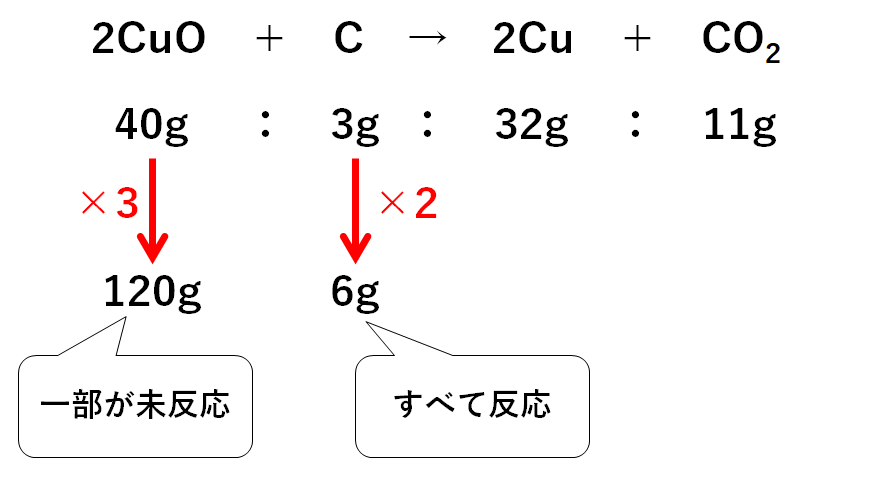



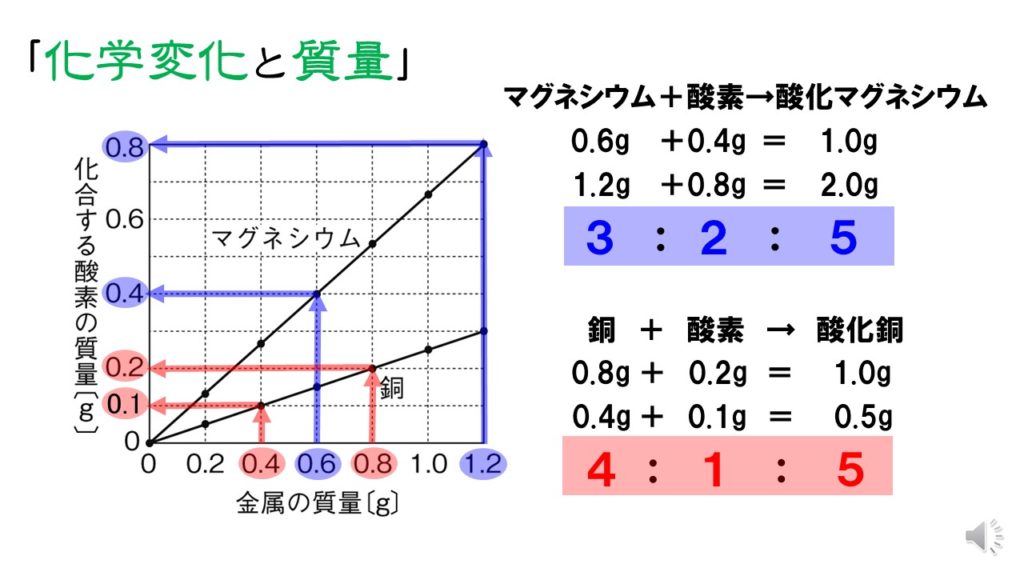
中2化学 定比例の法則 還元 中学理科 ポイントまとめと整理




分子量とは 単位もわかる 高校化学で必見の計算方法とは 高校生向け受験応援メディア 受験のミカタ
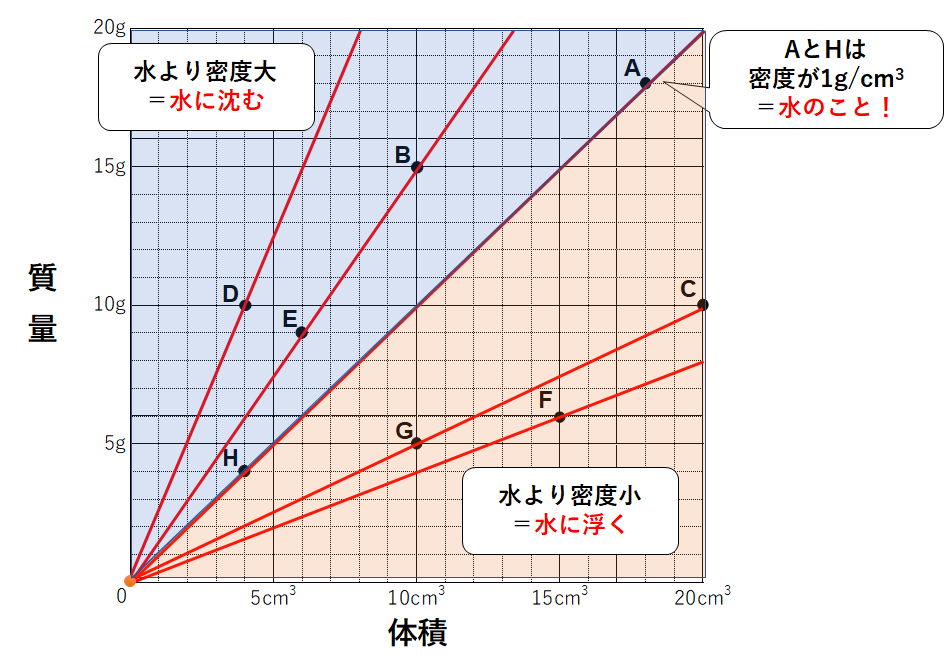



中1化学 密度 中学理科 ポイントまとめと整理




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく




中2理科 銅とマグネシウムの酸化と質量 計算問題 2学期中間テスト用 赤城 ᐡᐤᐡ



アボガドロ数の測定法




モル濃度計算の解き方 公式 希釈時の濃度 密度や質量パーセント濃度との変換など 化学のグルメ
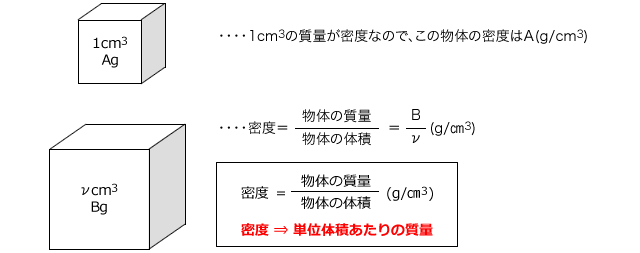



化学講座 第12回 濃度と密度 私立 国公立大学医学部に入ろう ドットコム




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく
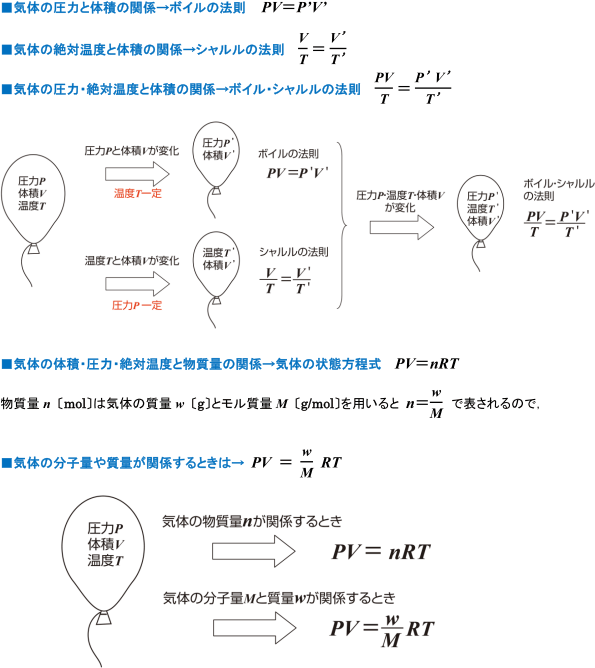



気体の性質 気体の計算の問題で どの式を使えばよいのかわかりません 化学 定期テスト対策サイト
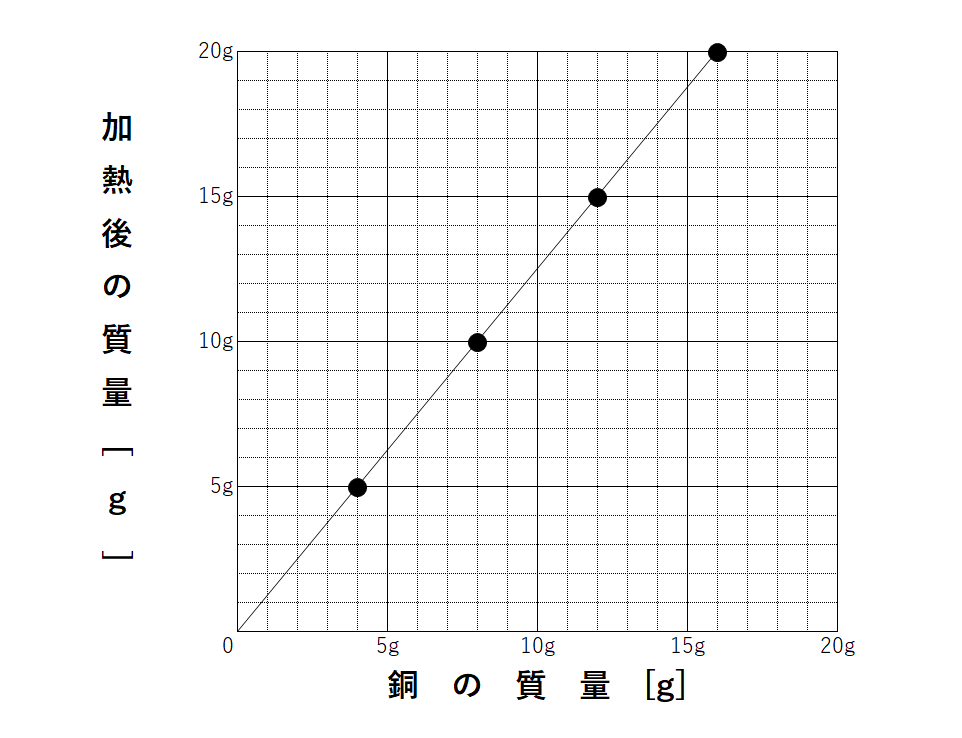



中2化学 定比例の法則 酸化 中学理科 ポイントまとめと整理




高校化学基礎 化学反応式と係数 映像授業のtry It トライイット



Qck0d2a9as2853cudbqy0lc6cfz4a0e7e Xyz Kiso Law Of Conservation Of Mass




高校化学基礎 ダースと本数 映像授業のtry It トライイット




物質量 Mol とモル質量と原子量の関係
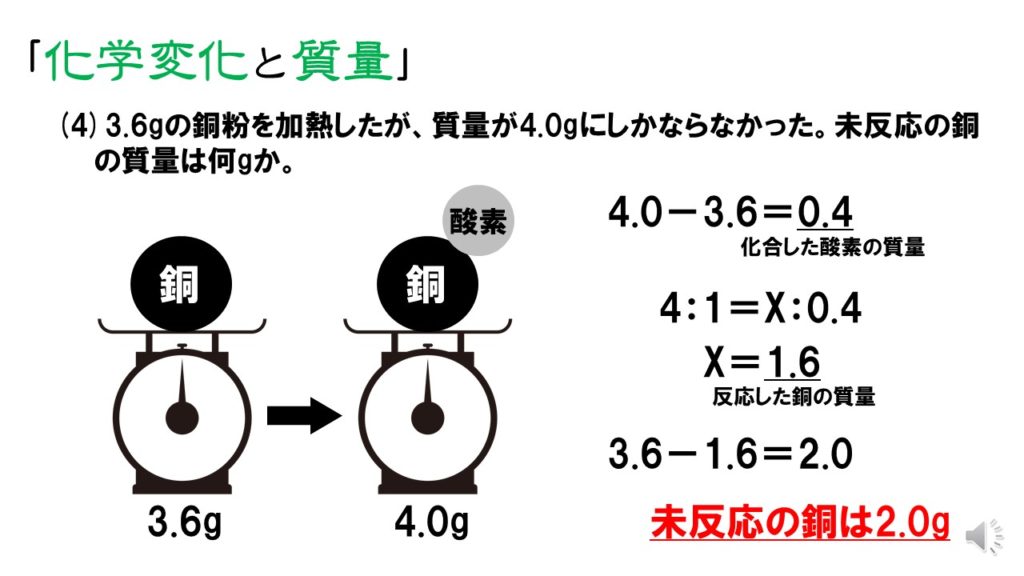



中2理科 化学変化と質量 銅とマグネシウムの計算 Pikuu
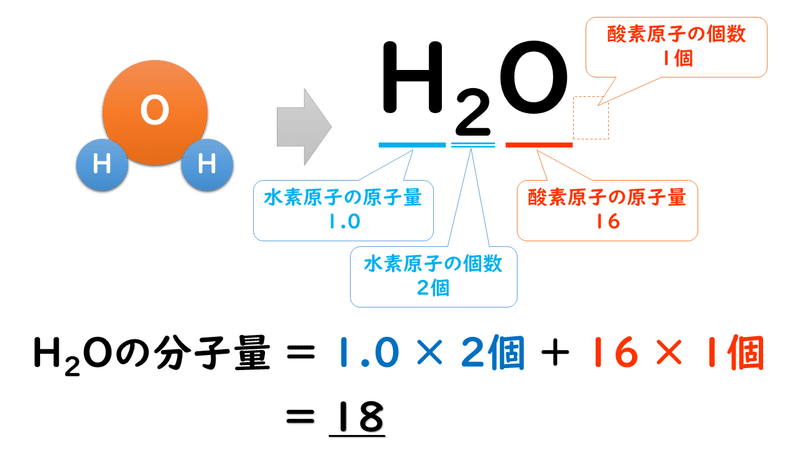



4 2 分子量 式量 おのれー Note



密度 体積 質量の換算式と求め方 計算問題 モッカイ
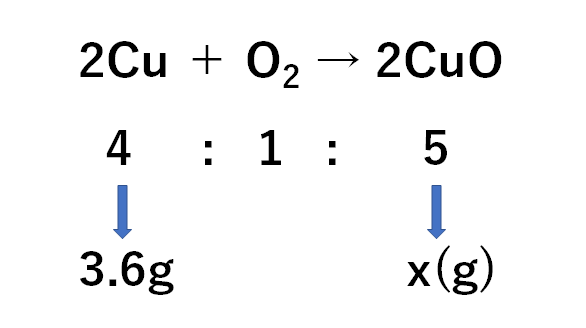



中2化学 定比例の法則 酸化 中学理科 ポイントまとめと整理




結晶水を含むときの溶解度と温度差による結晶析出量の求め方




アボガドロ定数とは 原子量 分子量 モルとの関係と物質量の求め方 高校生向け受験応援メディア 受験のミカタ




中1理科 密度の計算 3パターンの計算方法 Pikuu




高校生物基礎 腎臓のイヌリン濃縮率や原尿量などの計算問題の解き方 高校生物の学び舎



1
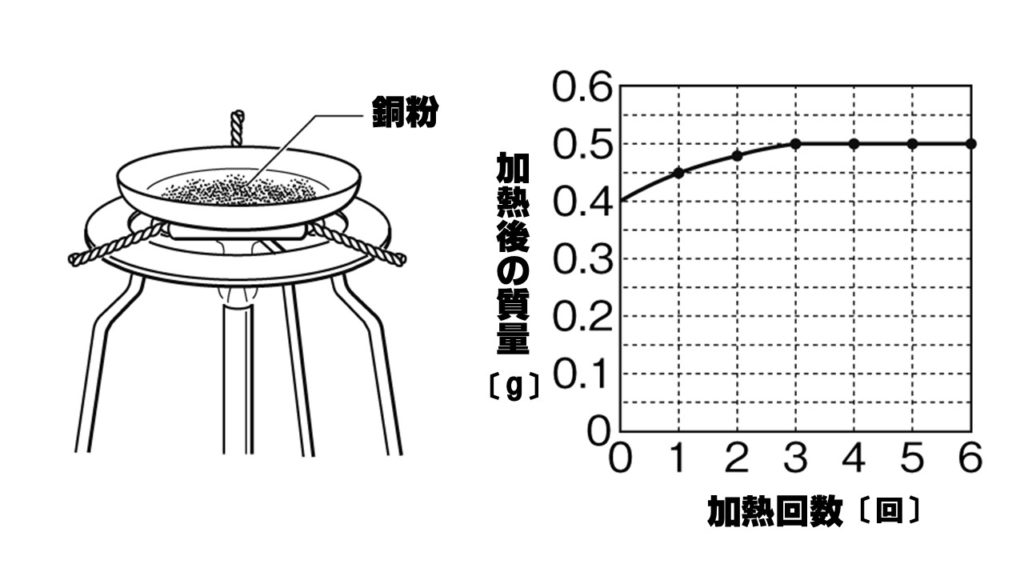



中2理科 化学変化と質量の計算問題 Examee




質量パーセント濃度の計算問題集 基本編 Menon Network
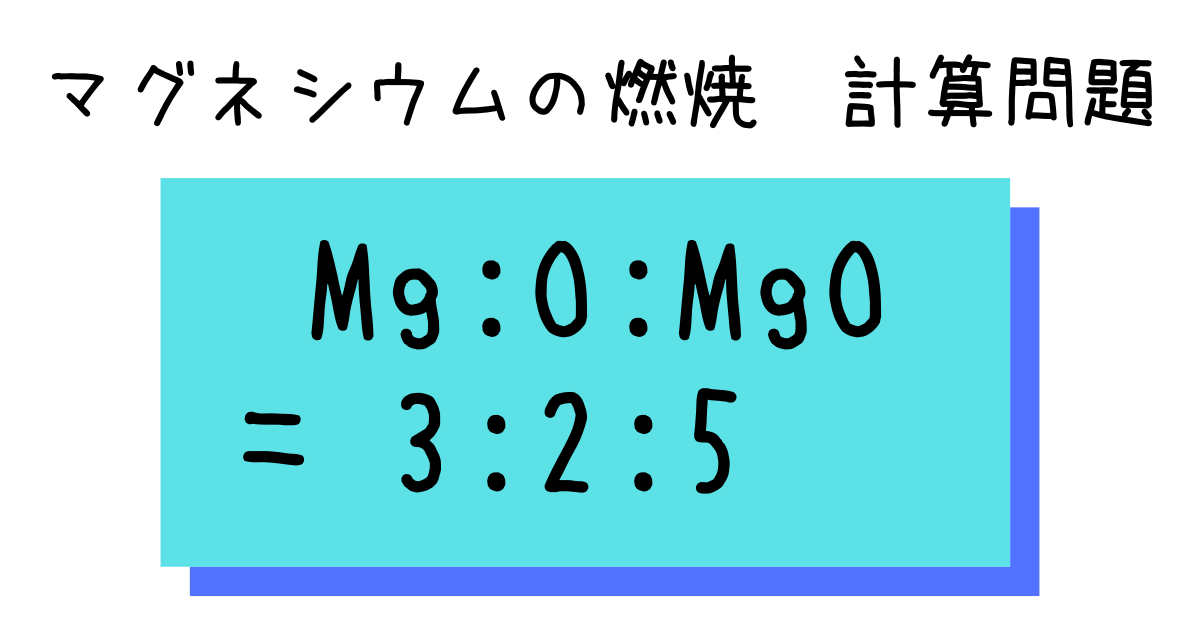



中2化学 マグネシウムの燃焼 計算問題 Hiromaru Note
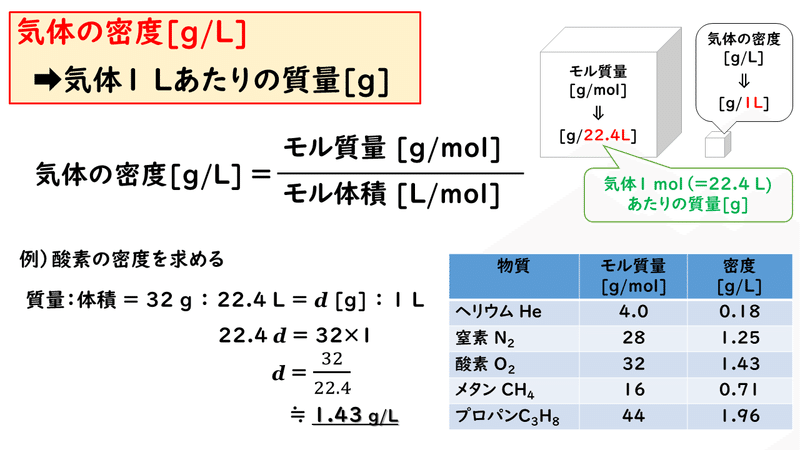



4 5 気体の密度と平均分子量 おのれー Note




質量分率と体積分率の変換 換算 方法 計算




アボガドロ定数とは 原子量 分子量 モルとの関係と物質量の求め方 高校生向け受験応援メディア 受験のミカタ



相対質量 原子量 分子量 式量 理解できてる 受験メモ
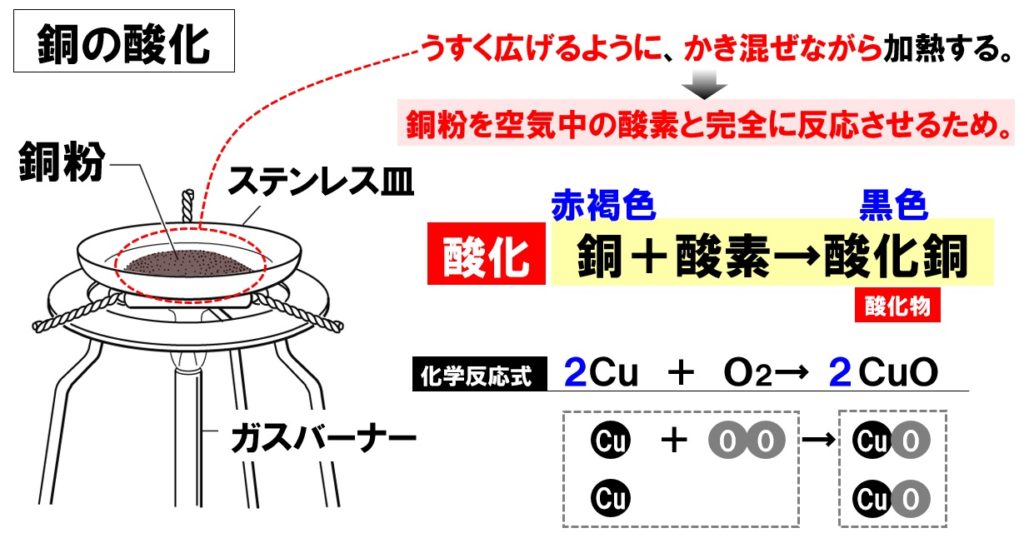



中2理科 化学変化と質量の計算問題 Examee




密度の公式 物質の密度の求め方は しみた の法則 中学理科 Yattoke 小 中学生の学習サイト




高校化学基礎 モル質量とは 映像授業のtry It トライイット



中2理科 化学変化と質量の計算問題 Examee



ラブリー理科 質量 の 求め 方 最高のぬりえ




気体の法則を使って計算しよう 空気の質量 について理系ライターが解説 ページ 2 2 Study Z ドラゴン桜と学ぶwebマガジン



アボガドロ数の測定法
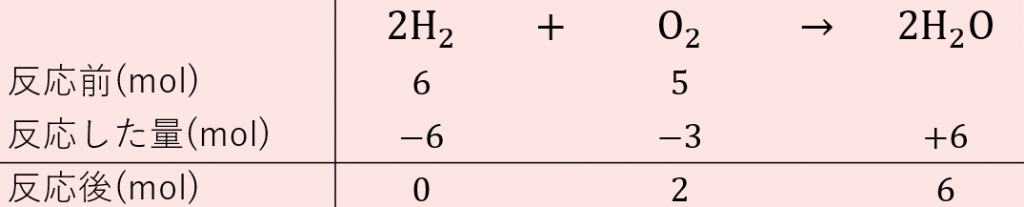



物質量molの超解説 理系ラボ
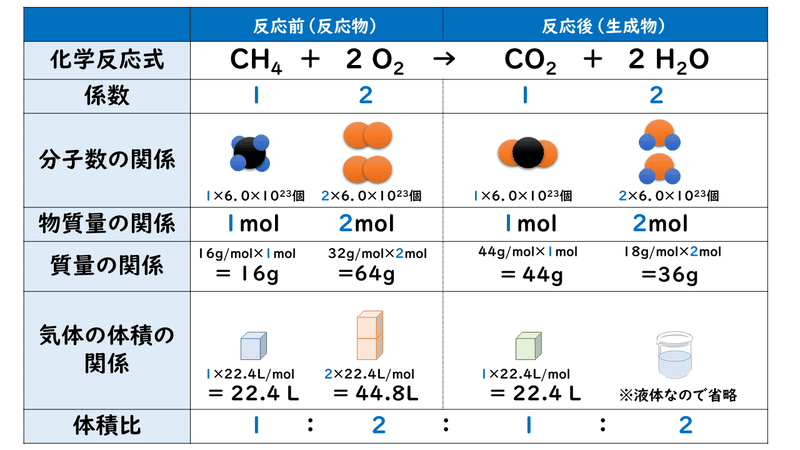



5 2 化学反応の量的関係 1 おのれー Note



物質量 の指導における イメージ化 化学授業実践記録 アーカイブ一覧 理科 高等学校 知が啓く 教科書の啓林館




4 6 溶液の濃度 おのれー Note
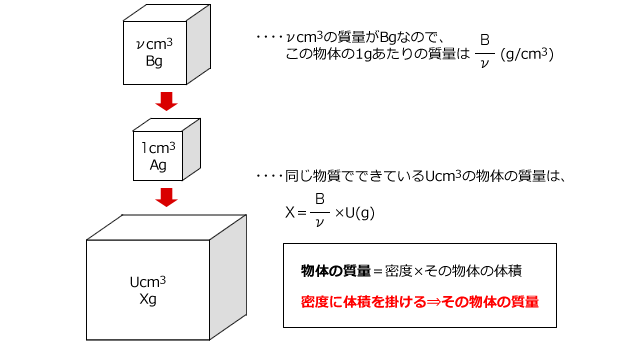



化学講座 第12回 濃度と密度 私立 国公立大学医学部に入ろう ドットコム




溶液の質量パーセント濃度の求め方と比重を利用した計算問題




溶液の性質 水和水をもつ固体の溶解度の求め方を教えてください 化学 定期テスト対策サイト




密度 体積 質量の換算式と求め方 計算問題 モッカイ




モル比熱 高校物理をあきらめる前に 高校物理をあきらめる前に
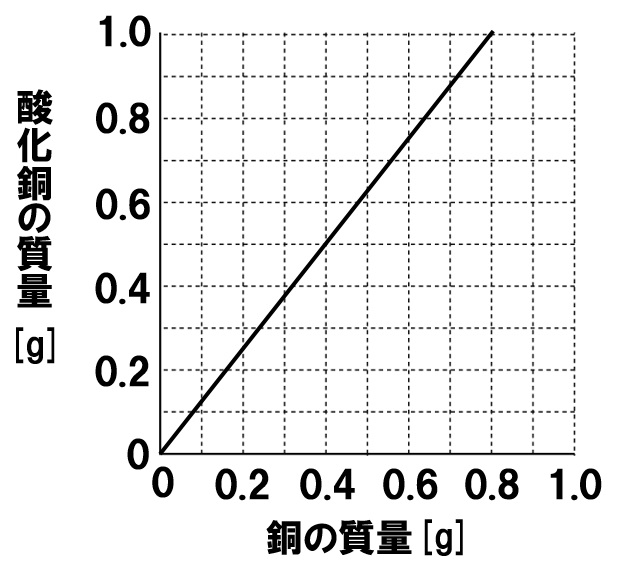



中2理科 化学変化と質量の計算問題 Examee




3分でわかる 質量パーセント濃度の求め方の計算公式 Qikeru 学びを楽しくわかりやすく



中1理科 密度の求め方3パターンの計算方法 Examee
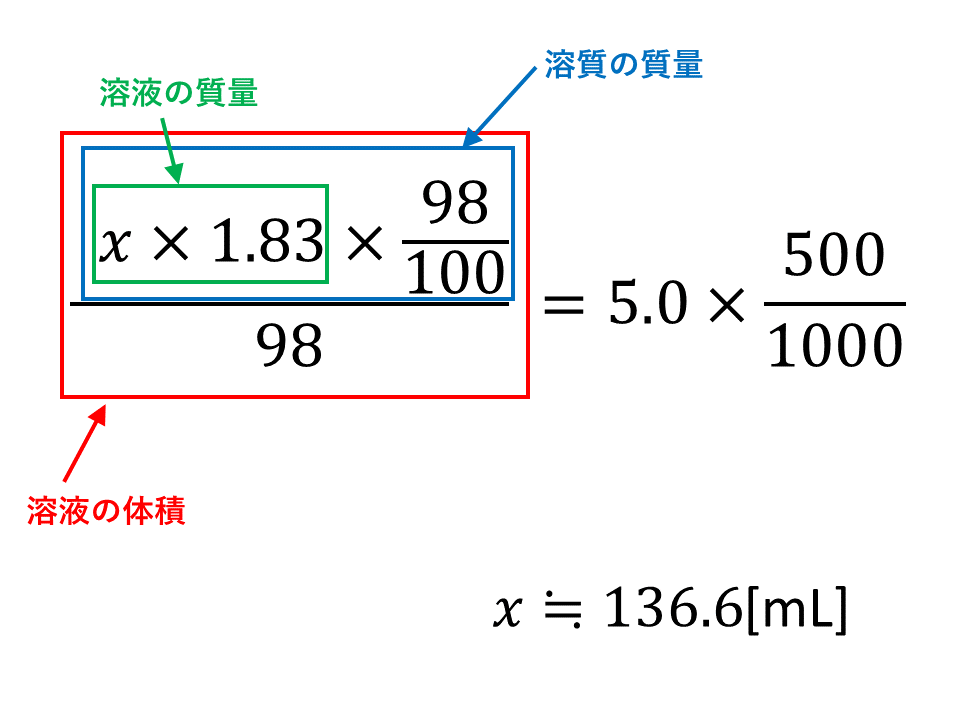



モル濃度と密度 質量パーセント濃度の考え方 Vicolla Magazine




質量パーセント濃度の計算問題集 応用編 Menon Network




高校化学基礎 密度とモル濃度 映像授業のtry It トライイット
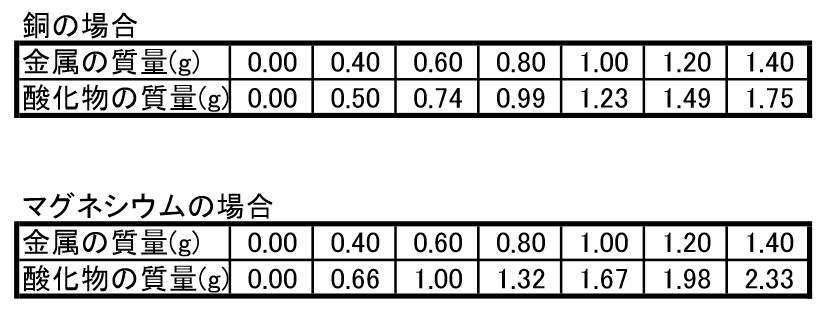



化学変化と物質の質量4 質量変化の規則性 後編 理科とか苦手で




高校化学基礎 モル質量の計算 練習編 映像授業のtry It トライイット




Iaqzqfvwejor6m




絶対質量と相対質量 相対質量の計算方法 絶対質量との変換




4 6 溶液の濃度 おのれー Note




分子量とは 単位もわかる 高校化学で必見の計算方法とは 高校生向け受験応援メディア 受験のミカタ




高校化学基礎 相対質量の計算 映像授業のtry It トライイット
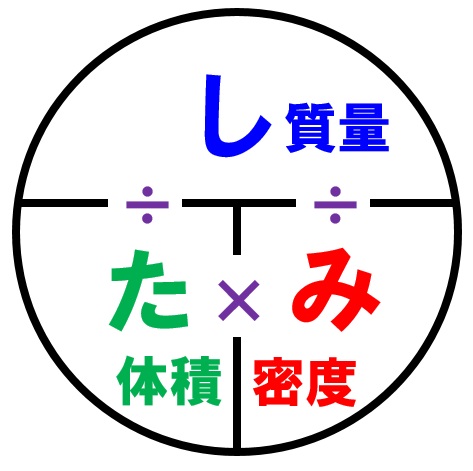



中1理科 密度の求め方3パターンの計算方法 Examee



質量と比重




質量パーセント濃度の求め方とモル濃度の違い
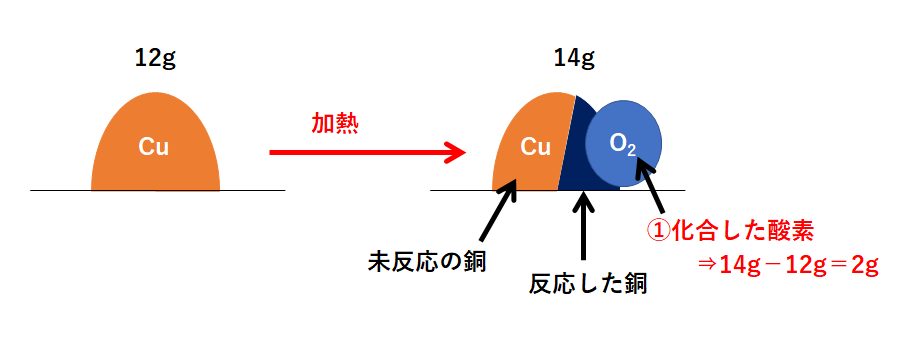



中2化学 定比例の法則 未反応 混合物 中学理科 ポイントまとめと整理




中学理科 3分でわかる 密度の求め方 出し方の計算公式 Qikeru 学びを楽しくわかりやすく




1分でわかる質量パーセント濃度の公式や求め方 基本を登録者数95万人人気講師がわかりやすく解説 ページ 4 4 Study Z ドラゴン桜と学ぶwebマガジン
コメント
コメントを投稿